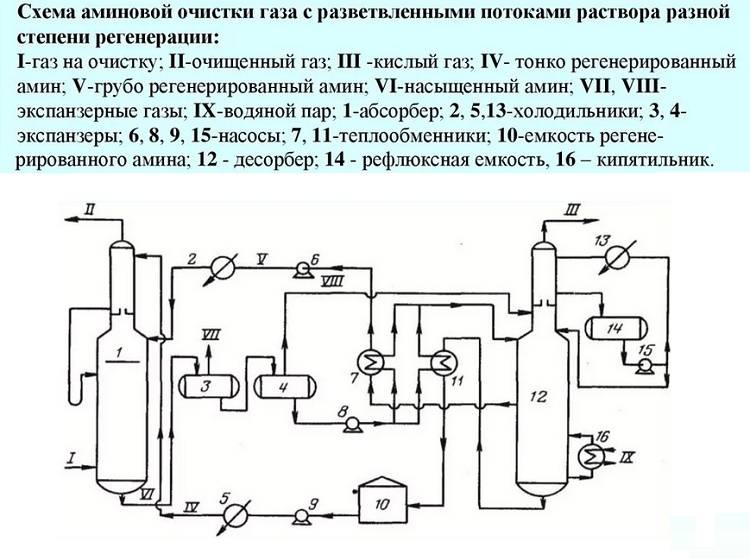
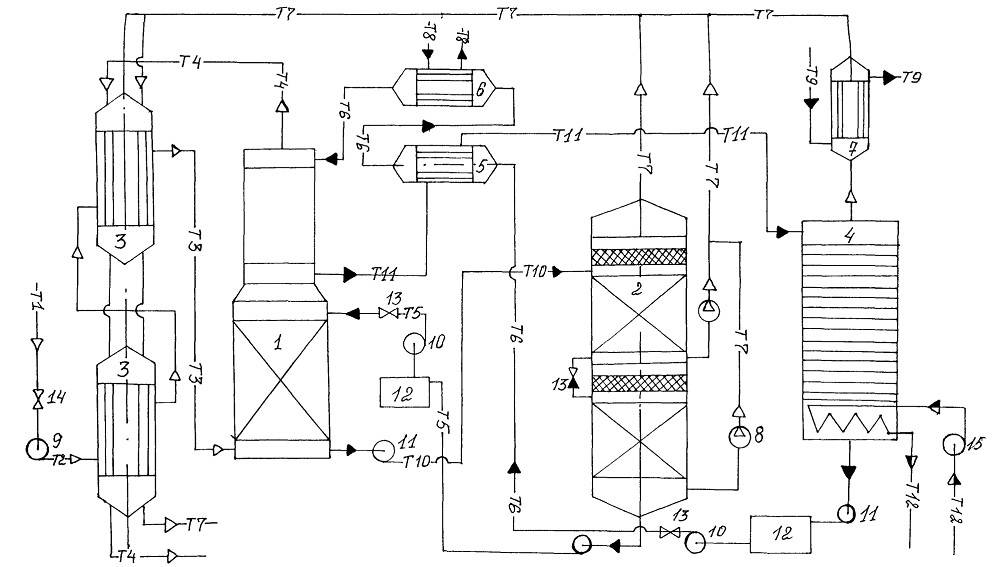
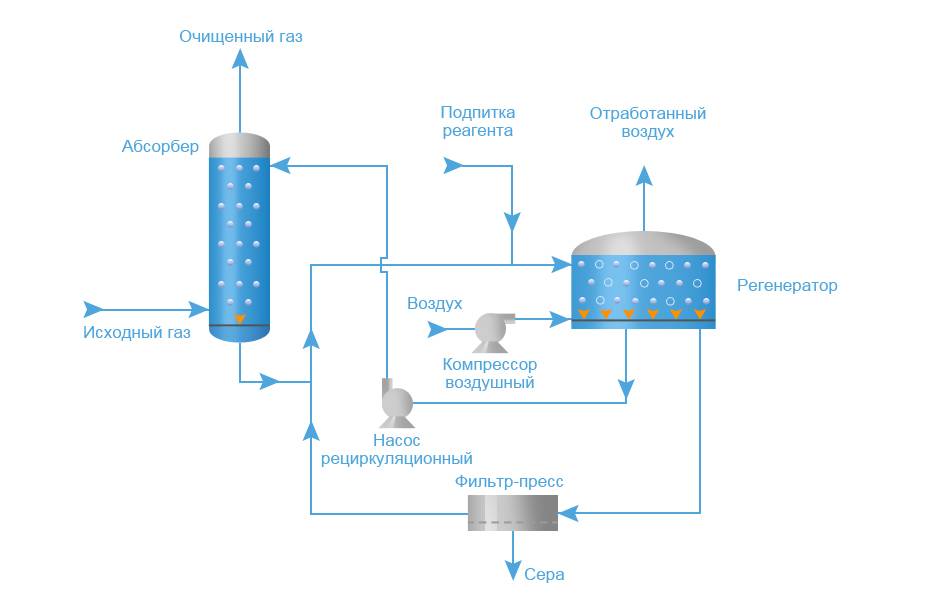
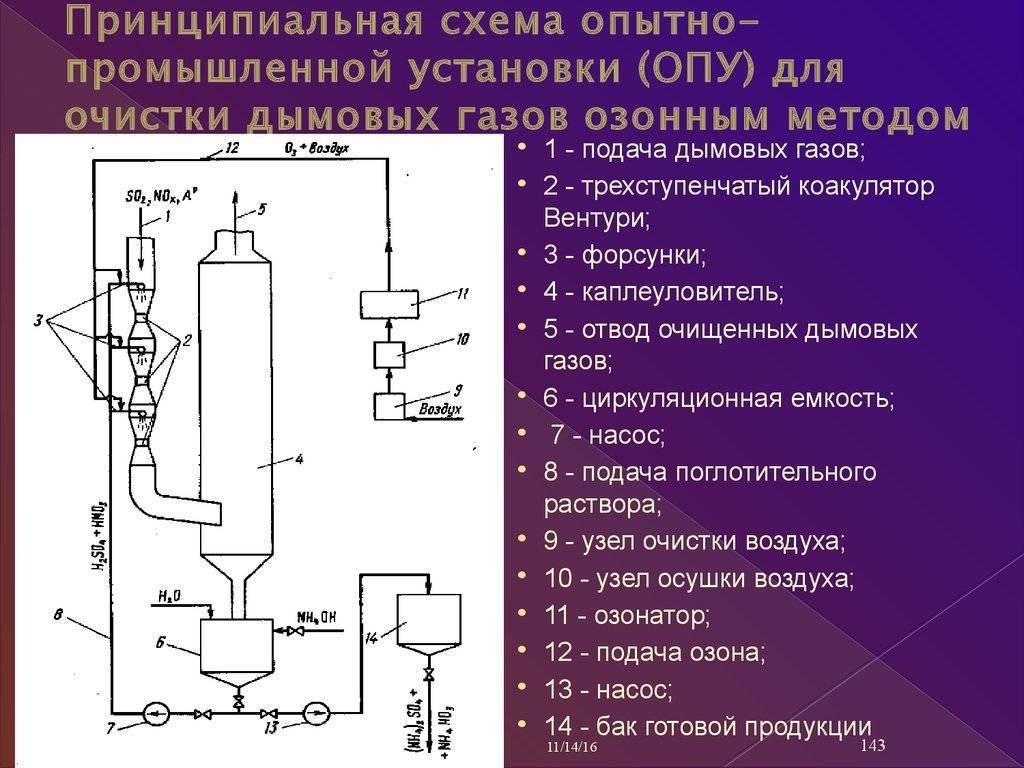
Амины
Концентрация амина в абсорбирующем водном растворе является важным параметром при разработке и функционировании процесса обработки аминного газа. В зависимости от того, для какого из следующих четырех аминов устройство было разработано, и для каких газов оно предназначено для удаления, это некоторые типичные концентрации амина, выраженные в процентах по массе чистого амина в водном растворе:
- Моноэтаноламин: около 20% для удаления H2S и CO2и около 32% для удаления только CO2.
- Диэтаноламин: от 20 до 25% для удаления H2S и CO2
- Метилдиэтаноламин: от 30 до 55% для удаления H2S и CO2
- Дигликоламин: около 50% для удаления H2S и CO2
Выбор концентрации амина в циркулирующем водном растворе зависит от ряда факторов и может быть совершенно произвольным. Обычно это делается просто на основе опыта. В число вовлеченных факторов входит то, обрабатывает ли аминовая установка сырые натуральный газ или же нефтеперерабатывающий завод побочные газы, содержащие относительно низкие концентрации как H2S и CO2 или обрабатывает ли установка газы с высоким содержанием CO2 такие как отходящие газы процесса парового риформинга, используемые в производство аммиака или дымовые газы из электростанции.
Оба H2S и CO2 являются кислыми газами и, следовательно, вызывают коррозию углеродистая сталь. Однако в установке обработки амином CO2 является более сильной кислотой из двух. ЧАС2S образует пленку сульфид железа на поверхности стали, которая защищает сталь. При обработке газов с высоким содержанием CO2часто используются ингибиторы коррозии, что позволяет использовать более высокие концентрации амина в циркулирующем растворе.
Еще одним фактором, влияющим на выбор концентрации амина, является относительная растворимость H2S и CO2 в выбранном амине. Выбор типа амина повлияет на требуемую скорость циркуляции раствора амина, энергозатраты на регенерацию и возможность выборочного удаления H2Только S или CO2 в одиночку при желании. Дополнительную информацию о выборе концентрации амина можно найти в книге Коля и Нильсена.
MEA и DEA
MEA и DEA – это первичные и вторичные амины. Они очень реакционны и могут эффективно удалять большой объем газа из-за высокой скорости реакции. Однако из-за стехиометрии емкость загрузки ограничена 0,5 моль CO.2 на моль амина. MEA и DEA также требуют большого количества энергии для удаления CO.2 во время регенерации, что может составлять до 70% общих эксплуатационных расходов. Они также более агрессивны и химически нестабильны по сравнению с другими аминами.
Четыре варианта очистки алконоламинами
Алконоламины или аминоспирты – это вещества, содержащие не только аминовую группу, но и гидроксигруппу.
Устройство установок и технологии очистки природного газа алканоламинами отличаются преимущественно способом подачи абсорбирующего вещества. Чаще всего в чистке газа с применением этого вида аминов используют четыре основных методики.
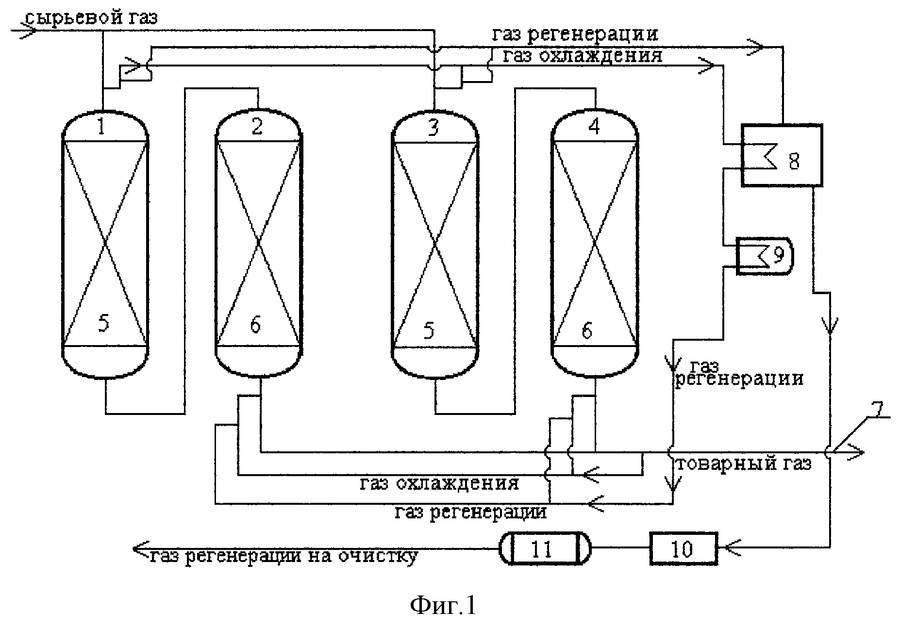
Первый способ. Предопределяет подачу активного раствора одним потоком сверху. Весь объем абсорбента направляется на верхнюю тарелку установки. Процесс очистки происходит при температурном фоне не выше 40ºС.
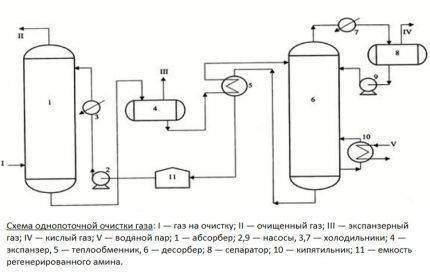 Простейший способ очистки предполагает подачу активного раствора одним потоком. Эта методика применяется, если примесей в газе незначительное количество
Простейший способ очистки предполагает подачу активного раствора одним потоком. Эта методика применяется, если примесей в газе незначительное количество
Эта методика обычно используется при незначительном загрязнении сероводородными соединениями и углекислотой. Суммарный тепловой эффект для получения товарного газа при этом, как правило, невысок.
Второй способ. Этот вариант очистки применяется при высоком содержании сероводородных соединений в газообразном топливе.
Реактивный раствор в этом случае подают в два потока. Первый, объемом примерно 65-75% общей массы, направляется в середину установки, второй поставляется сверху.
Аминовый раствор стекает вниз по тарелкам и встречается с восходящими газовыми потоками, которые нагнетаются на нижнюю тарелку абсорбирующей установки. Перед подачей раствор разогревается не более чем до 40ºС, но в ходе взаимодействия газа с амином температура значительно повышается.
Чтобы из-за повышения температуры не падала эффективность чистки, избыток тепла отводится вместе с отработанным раствором, насыщенным сероводородом. А вверху установки производится охлаждение потока с целью извлечения остатков кислых составляющих вместе с конденсатом.
 Второй и третий из описанных способов предопределяет подачу абсорбирующего раствора двумя потоками. В первом случае реактив подают одной температуры, во втором – разной
Второй и третий из описанных способов предопределяет подачу абсорбирующего раствора двумя потоками. В первом случае реактив подают одной температуры, во втором – разной
Это экономичный способ, позволяющий сократить расход как энергии, так и активного раствора. Дополнительный подогрев не производится ни на одном этапе. По технологической сути он является двухуровневой очисткой, предоставляющей возможность с наименьшими потерями подготовить товарный газ к подаче в магистраль.
Третий способ. Предполагает поставку абсорбера в очищающую установку двумя потоками разной температуры. Методика применяется, если кроме сероводорода и углекислоты в сыром газе есть еще и CS2, и COS.
Преобладающая часть абсорбера, примерно 70-75%, разогревается до 60-70ºС, а оставшаяся доля только до 40ºС. Подаются потоки в абсорбер так же, как в вышеописанном случае: сверху и в середину.
Формирование зоны с высокой температурой дает возможность быстро и качественно извлечь органические загрязнения из газовой массы внизу очищающей колонны. А вверху диоксид углерода и сероводород осаждаются амином стандартной температуры.
Четвертый способ. Эта технология предопределяет подачу водного раствора амина двумя потоками с разной степенью регенерации. То есть один поставляется в неочищенном виде, с содержанием сероводородных включений, второй – без них.
Первый поток нельзя назвать полностью загрязненным. Он только частично содержит кислые компоненты, потому что часть из них удаляется в ходе охлаждения до +50º/+60ºС в теплообменнике. Этот поток раствора забирается с нижней насадки десорбера, охлаждается и направляется в среднюю часть колонны.
 При значительном содержании сероводородных и углекислых компонентов в газообразном топливе очистку производят двумя потоками раствора с разной степенью регенерации
При значительном содержании сероводородных и углекислых компонентов в газообразном топливе очистку производят двумя потоками раствора с разной степенью регенерации
Глубокую очистку проходит только та часть раствора, которую нагнетают в верхний сектор установки. Температура этого потока обычно не превышает 50ºС. Здесь выполняется тонкая чистка газообразного топлива. Эта схема позволяет сократить расходы как минимум на 10 % за счет сокращения расхода пара.
Понятно, что способ очистки выбирают, исходя из наличия органических загрязнений и экономической целесообразности. В любом случае разнообразие технологий позволяет подобрать оптимальный вариант. На одной и той же установке аминовой обработки газа можно варьировать степень очистки, получая голубое горючее с нужными для работы газовых котлов, плит, обогревателей характеристиками.
Примерное объяснение
Если подумать о газированной минеральной воде, принцип поглощения можно сделать более ощутимым:
Если бутылка с минеральной водой холодная и неоткрытая (внутри высокое давление), в воде содержится много CO 2 в виде угольной кислоты. В случае аминовой очистки это представляет собой абсорбер.Если баллон теперь открыт (более низкое давление) и хранится неохлаждаемым (более высокая температура), CO 2 высвобождается из связки и попадает в окружающую среду. При аминовой очистке это десорбер.Самое большое отличие состоит в том, что аминовая очистка представляет собой смесь воды и аминов, которые могут химически связывать значительно больше CO 2, и во время регенерации в десорбере необходимо добавлять меньше тепла.
Процесс очистки: польза и вред
Каждое из месторождений характеризуется своими параметрами сероводородных соединений. Извлеченные на поверхность земли, компоненты вредят окружающей среде. Высокая концентрация серы замедляет (или делает невозможным) выполнение следующих этапов переработки и транспортировки газа.
Сероводородные соединения:
- ядовиты для человеческого организма;
- разъедают газоперерабатывающего оборудования и стенки трубопроводов;
- препятствуют работе катализаторов, которые используются при синтезе газа.
Согласно нормативам, в магистрали доля тиоловой серы не должна превышать 16 мг/м3, сероводорода – 7 мг/м3. Перед отправкой потребителю природное сырье очищают от серосодержащих соединений.
Широкое использование извлеченных серосодержащих добавок повышает рентабельность добычи. Кислые компоненты используют:
- при изготовлении сухого льда для заведений общественного питания;
- на предприятиях химической промышленности для получения углекислого газа, серной кислоты;
- как удобрение – при обработке земли и уходе за растениями.
Необходимость фильтрации кислых примесей
Кислые газы (англ. acid gases / acid components) – это газообразные химические элементы и молекулярные соединения, обладающие высокой коррозионной активностью. Под кислыми компонентами газовых сред в промышленной газоочистке также могут подразумеваться жидкие (парообразные или аэрозольные) вещества, оказывающие сильное деструктивное воздействие на металлоконструкции, моторы, газоходы, иные вспомогательные металлические узлы и агрегаты.
Налет хлоридов / оксихлоридов на тестовой прокладке трубы газохода
Если же речь идет о кислотных составляющих газов, использующихся или очищающихся до уровня топлив, то нежелательные примеси рассматриваются как балластные, (т.е. снижающие калорийность / температуру горения и другие полезные свойства газовой смеси).
Помимо прочего, почти все кислые компоненты – пожалуй, кроме CO2 – биологически активны, ядовиты: вызывают удушье, спазмы дыхательных путей, повреждения кожных покровов, слизистых оболочек, нервной ткани, (иногда – всё сразу).
Экономическая целесообразность
Выбранный процесс должен быть экономически эффективным в соответствии с различными спецификациями и требованиями. Во всем мире правила обычно ограничивают сжигание H2S.

Очистить газовые потоки, содержащие очень низкие концентрации H2S, можно разными способами, в зависимости от общих условий. Если поток кислого газа содержит более 30-45 кг серы в день в форме H2S в сырьевом, для очистки потока кислого газа обычно выбирают регенеративный химический абсорбент. Для кислого газа, имеющего очень низкое содержание H2S , обычно используется химический нейтрализатор. В таких случаях химическое вещество расходуется, и метод окончательного удаления отработанного химического вещества является предметом обсуждения.
Процесс
История
Первый патент, связанный с удалением кислых газов путем абсорбции аминоспиртом, был подан RR Bottoms в 1930 году. Триэтаноламин , который был первым амином, производимым в промышленных масштабах , использовался в первых газоперерабатывающих установках. Другие амины оцениваются в этом направлении, как только их производство становится промышленным. Диэтаноламин (ДЭА), то этаноламин (МЕА) и N-метил диэтаноламин (МДЭА), которые являются гораздо более эффективными, заменить его быстро. Диизопропиламин (DIPA) на короткое время используется , прежде чем отказаться в пользу МДЭА.
В начале 1950-х годов открытие газового месторождения Лак побудило компанию Total к инновациям, направленным на снижение экстремальной кислотности добываемого газа: он содержал почти 16% сероводорода (H 2 S) и 10% диоксида углерода (CO 2). ВАпрель 1957 г.После серьезных исследований материалов и процессов введена в эксплуатацию первая установка подготовки газа мощностью 1 миллион кубических метров газа в сутки, основанная на использовании диэтаноламина (ДЭА). Испытываются различные амины: в 1978 году диэтаноламин (МДЭА) был принят для обработки некоторых газов, богатых сероводородом.
В начале 1970-х годов немецкая компания BASF стремилась улучшить синтез аммиака , работая над выходом процесса Габера-Боша . Этому процессу, в ходе которого из газовой смеси азота и водорода синтезируется аммиак , предшествует этап удаления диоксида углерода. Идея осуществления этого вывода реакцией с аминами оказывается успешной. Впоследствии он был улучшен с использованием активированного N- метилдиэтаноламина (aMDEA), который заменяет этаноламин (MEA) или процесс карбоната калия .
Принцип
Газы, обычно удаляемые аминами, являются кислыми газами, такими как диоксид серы (SO 2), хлористый водород (HCl), диоксид азота (NO 2), цианистый водород (HCN), угольная кислота (H 2 CO 3) и т. д. но также сероводород (H 2 S) и диоксид углерода (CO 2), гораздо чаще. Эти газы являются общими в промышленных процессах по органической химии .
Химические реакции различаются в зависимости от типа удаляемого амина и кислого газа. В примере с обычным амином, этаноламином , обозначается RNH 2., реагируя с сероводородом, химическая реакция записывается следующим образом:
RNH 2 + H 2 S RNH 3 + + SH –⇌{\ displaystyle \ rightleftharpoons}
а для CO 2 :
RNH 2 + CO 2 RNHCOO – + H +⇌{\ displaystyle \ rightleftharpoons}
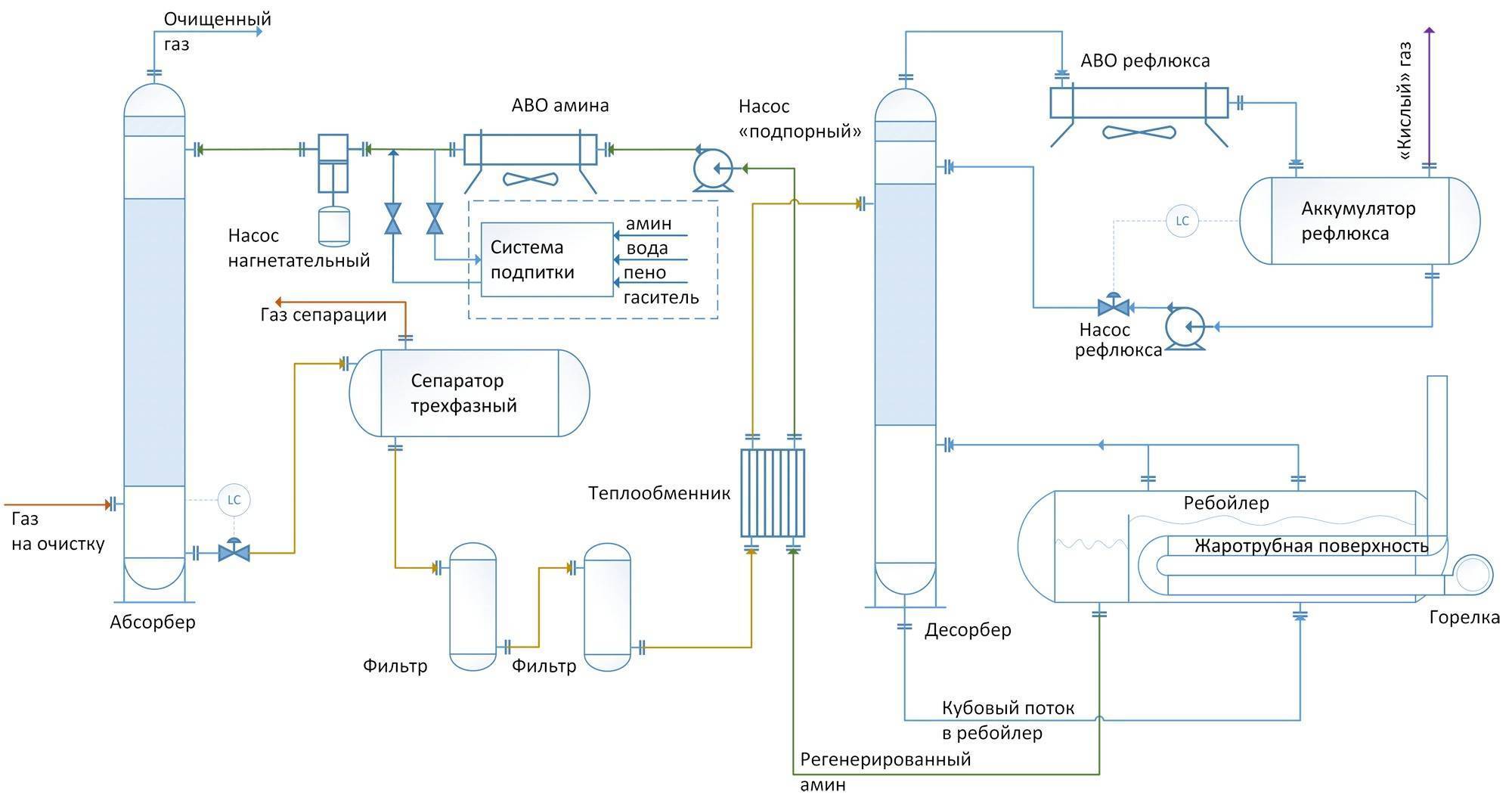
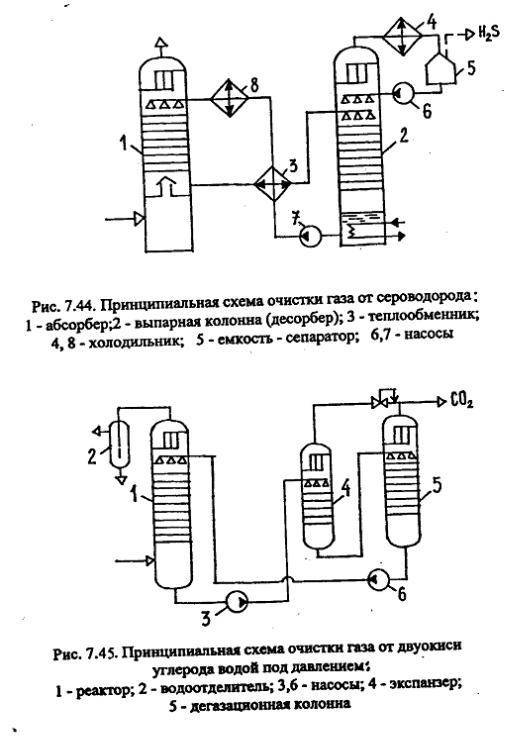
Установка аминовой обработки обычно состоит из двух химических реакторов , абсорбера и регенератора . В абсорбере нисходящий поток амина встречает восходящий поток газовой смеси и соединяется с содержащимися в нем кислыми газами. «Мягкая» газовая смесь оставляет абсорбер свободным от кислот, «богатый» амин течет, унося с собой кислые газы. В регенераторе богатый амин последовательно нагревается в отпарной колонне (тип испарителя ) и бойлере, так что пары, богатые кислотами, удаляются. Амин, который стал «обедненным» кислотами, охлаждается богатым амином, полученным из абсорбера. Затем холодный бедный амин может вернуться в абсорбер для промывки газа.
Негативные эффекты сероводорода и необходимость очистки газовоздушных сред от H2S
Сернистый водород – одно из простых и широко распространенных соединений, которое в небольших количествах встречается повсеместно. Велика роль эндогенного сероводорода в живых организмах, где он выполняет множество важных нейробиологических функций. Используется он и в лечебных ваннах, в микроскопических объемах благотворно влияя на организм человека.
Впрочем, когда речь идет о такой технологической процедуре как мокрая или сухая очистка воздуха от сероводорода, ясно – что высокая концентрация данного соединения несет лишь сугубо негативные последствия для здоровья, жизни и экологии планеты.
Последствия кислотных дождей, содержащих сернистые компоненты
В значительных объемах чистый сероводород и его производные образуются на гидрометаллургических фабриках, предприятиях органического синтеза, аграрных и химических заводах – при производстве серной кислоты, серы, селитры, серосодержащих удобрений.
В составе дымовых газов H2S – постоянный спутник всех без исключения выбросов от сгорания органического сырья – наряду с оксидами серы, окислами азота, соляной кислотой, фенолами, монооксидом углерода.
Очистка биогаза от сероводорода и углекислого газа – одна из насущных проблем, стоящих перед операторами промышленных биометановых электростанций.
Выполненный проект: внедрение системы утилизации сероводорода на гидрометаллургическом предприятии
В опасной концентрации запах газообразного дигидросульфида – тошнотворный «аромат» гниющего мяса или стухших яиц – практически мгновенно перестает ощущаться. Это таит огромную опасность, поскольку H2S быстро парализует обонятельные нервы, и человек продолжает вдыхать из воздуха вредное соединение, уже не ощущая его запаха.
Установки очистки газа от сероводорода востребованы также и в силу его разрушительного воздействия на технические коммуникации. Индивидуально или в составе дымов, сульфид водорода и другие сернистые соединения вызывают сильнейшую коррозию трубопроводов, резервуаров, фитингов, компрессоров и любого другого оборудования, не обладающего специальной антикоррозийной защитой.
Помимо этого, сернистый водород пожаро- и взрывоопасен: 4%-ое его присутствие в воздушной среде может вызвать катастрофические последствия. Так, 27 ноября 2018 года на химическом заводе в восточном Китае, (провинция Хэбэй), по крайней мере, 23 человека погибли и более 22 получили тяжелые ранения в результате самопроизвольного взрыва H2S.
Двойной удар вызывает сероводород, присутствующий в отходящих дымовых газах. С одной стороны, на пути следования по тракту он негативно воздействует на коммуникационные, технические и выхлопные системы предприятий, с другой – выбрасывается в атмосферу, после чего может трансформироваться (через окисление) в серную кислоту и выпадать в виде кислотных дождей, опасность которых для экологии сложно преувеличить.
Симптомы отравления дигидросульфидом
Это интересно: Как работает термоодеяло для газовых баллонов: устройство, назначение и рекомендации по выбору
Рекомендации
- ^ а б c d Артур Коль; Ричард Нильсон (1997). Очистка газа (5-е изд.). Издательство Gulf Publishing. ISBN 0-88415-220-0.
- ^ Gary, J.H .; Хандверк, Г. (1984). Технология и экономика нефтепереработки (2-е изд.). Марсель Деккер, Inc. ISBN 0-8247-7150-8.
- ^ США 4080424, Лорен Н. Миллер и Томас С. Завацки, “Процесс удаления кислых газов из газовых смесей”, выпущенный 21 марта 1978 г., передан Институту газовых технологий.
- ^ Бейкер, Р. В. (2002). «Будущие направления технологии мембранного разделения газов». Ind. Eng. Chem. Res. 41 (6): 1393–1411. Дои:10.1021 / ie0108088.
- ^ Оенекан, Бабатунде; Рошель, Гэри Т. (2007). “Альтернативные конфигурации стриппера для CO2 Улавливание водными аминами “. Журнал Айше. 53 (12): 3144–154. Дои:10.1002 / aic.11316.
- ^ а б То же, Рафаэль (2006). “Опытно-промышленные исследования CO2 Захват производительности Aqueoues MEA и смешанных растворителей MEA / MDEA в Университете Реджайны2 Завод по разработке технологии улавливания и пограничная плотина CO2 Захват демонстрационного завода “. Ind. Eng. Chem. Res. 45 (8): 2414–2420. Дои:10.1021 / ie050569e.
- ^ Отчет о производстве серы посредством Геологическая служба США
- ^ Обсуждение рекуперированной серы как побочного продукта
- ^ Абацоглу, Николас; Бойвин, Стив (2009). «Обзор процессов очистки биогаза». Биотопливо, биопродукты и биопереработка. 3 (1): 42–71. Дои:10.1002 / bbb.117. ISSN 1932-104X.
- ^ Рошель, Г. Т. (2009). «Аминовая очистка CO2 Захватывать”. Наука. 325 (5948): 1652–1654. Дои:10.1126 / science.1176731. ISSN 0036-8075. PMID 19779188. S2CID 206521374.
- ^ а б Фолгер, П. (2009). «Улавливание углерода: оценка технологии». Отчет исследовательской службы Конгресса для Конгресса. 5: 26–44.
- ^ а б c У, Инь; Кэрролл, Джон Дж. (5 июля 2011 г.). Связывание диоксида углерода и связанные с ним технологии. Джон Вили и сыновья. С. 128–131. ISBN 978-0-470-93876-8.
Технические характеристики установки для очистки газов от сероводорода
- Производительность, с которой выполняется очистка попутного газа: 20/100/200 нм3/ч
- Исходная концентрация сероводорода (H2S) на входе: до 5% об.
- Концентрация сероводорода на выходе после сероочистки: не более 0,01% об.
- Энергопотребление в рабочем режиме: 3 кВт/ч
- Возможная пиковая нагрузка до 5 кВт
- Сопротивление установки 20 кПа.
- Объём рабочего раствора рассчитан на 2 месяца работы
- Срок службы установки 5 лет.
- Масса: 1 450 кг.
Внешние габариты рамы:
Длина 6000 мм, Высота 2200 мм, ширина 2000 мм
+ёмкость раствора 10 м3 (3 Х 2 м) + Ёмкость приёма серы (2 Х 2 м)
Возможен монтаж в контейнер для установки и система вентиляции, при необходимости.
Выбор абсорбента для процесса очистки
Желаемыми характеристиками абсорбента являются:
- необходимость удаления сероводорода H2S и других соединений серы.
- поглощение углеводородов должно быть низким.
- давление паров абсорбента должно быть низким, чтобы минимизировать потери абсорбента.
- реакции между растворителем и кислыми газами должны быть обратимыми, чтобы предотвратить разложение абсорбента.
- абсорбент должен быть термически стабильным.
- удаление продуктов разложения должно быть простым.
- поглощение кислого газа на единицу циркулирующего абсорбента должно быть высоким.
- потребность в тепле для регенерации или удаления абсорбента должна быть низкой.
- абсорбент должен быть неагрессивным.
- абсорбент не должен пениться в абсорбере или десорбере.
- желательно избирательное удаление кислых газов.
- абсорбент должен быть дешевым и легкодоступным.
К сожалению, нет ни одного абсорбента, который обладает всеми желаемыми характеристиками. Это делает необходимым выбор абсорбента, который лучше всего подходит для обработки конкретной смеси кислых газов из различных доступных абсорбентов. Кислые смеси природного газа различаются по:
- содержанию и соотношению H2S и CO2
- содержанию тяжелых или ароматических соединений
- содержанию COS, CS2 и меркаптанов
Хотя кислый газ в основном очищается абсорбентами, для слабо кислого газа может быть более экономичным использование абсорбентов-поглотителей или твердых агентов. В таких процессах соединение химически реагирует с H2S и расходуется в процессе очистки, требуя периодической замены очищающего компонента.
Процедура
Для аминовой очистки используются слабощелочные водные растворы аминов (в основном производных этаноламина), которые обратимо химически абсорбируют кислые компоненты газа . В абсорбер (примерно 40 ° C) подается свежий раствор амина (около 8 бар) под небольшим давлением (примерно 8 бар) из головки при низкой температуре. Очищаемый газ подается в разделительную колонну снизу . Химическая реакция абсорбированного CO 2 с раствором амина выделяет энергию в виде тепла. Очищенный газ выходит из колонны вверху, а загруженное детергент (раствор амина) закачивается в десорбер внизу колонны.
В десорбере при высокой температуре (использование тепловой энергии) и низком давлении происходит реакция химического равновесия, и связанный кислый газ удаляется из моющего средства. Таким образом, чистый газ (с влажными компонентами) можно отводить в верхней части десорбера. Пропорции моющего средства и воды отделяются от газового потока конденсатором и возвращаются в колонну.
Последующая регенерация моющего средства позволяет извлекать связанный газ в высокой концентрации. Это делает более позднее использование материала z. B. Возможно использование CO 2 или H 2 S ( процесс Клауса ). Это невозможно с другими методами, такими как промывка водой под давлением .
В основном используются диэтаноламин и моноэтаноламин , но также распространены метилдиэтаноламин , диизопропиламин , диизопропаноламин и дигликольамин :
- Моноэтаноламин (MEA) поглощает только CO 2 с энтальпией реакции около 85 кДж / моль.
- Диэтаноламин (ДЭА)
- Метилдиэтаноламин (МДЭА) поглощает H 2 S и CO 2 с энтальпией реакции примерно 62 кДж / моль.
- Дигликоламин (DGA)
Часто смеси этих упомянутых аминов также используются для использования синергетических эффектов , таких как каталитический эффект для реакций моющего средства.
Важным критерием оценки для различных смесей является тепловая мощность, которая используется в испарителе для регенерации кислого газа из моющего средства. Это можно выразить через количество тепла, поглощенного CO 2 .
Реакции
Здесь показаны чистые реакции H 2 S и CO 2 .
- Р.-NЧАС2 + ЧАС2С. ⇌ Р.-NЧАС3+ + ЧАСС.-{\ Displaystyle \ mathrm {R {-} NH_ {2} \ + \ H_ {2} S \ \ rightleftharpoons \ R {-} NH_ {3} ^ {+} \ + \ HS ^ {-}}}
- Р.-NЧАС2 + С.О2 ⇌ Р.-NЧАСС.ОО- + ЧАС+{\ Displaystyle \ mathrm {R {-} NH_ {2} \ + \ CO_ {2} \ \ rightleftharpoons \ R {-} NHCOO ^ {-} \ + \ H ^ {+}}}
Сеть ответа
Ионизация воды:
ЧАС2О↽–⇀ЧАС++ОЙ-{\ displaystyle {\ ce {H2O <=> H + + OH-}}}
Ионизация растворенного H 2 S
ЧАС2С.↽–⇀ЧАС++HS-{\ displaystyle {\ ce {H2S <=> H + + HS-}}}
Гидролиз и ионизация растворенного CO 2
CO2+ЧАС2О↽–⇀HCO3-+ЧАС+{\ displaystyle {\ ce {CO2 + H2O <=> HCO3- + H +}}}
Протонирование амина
RNH2+ЧАС+↽–⇀RNH3+{\ Displaystyle {\ ce {RNH2 + H + <=> RNH3 +}}}
Образование карбаматов
RNH2+CO2↽–⇀RNHCOO-+ЧАС+{\ displaystyle {\ ce {RNH2 + CO2 <=> RNHCOO- + H +}}}
Эти реакции описывают возможные пути связывания CO 2 или H 2 S. Согласно закону Генри результирующие равновесные концентрации зависят от парциальных давлений газов. Образовавшиеся карбаматы представляют собой группу стабильных продуктов реакции, которые снова растворяются только в десорбере.
Когда CO 2 абсорбируется смесью амин / вода, CO 2 сначала растворяется в воде и образует угольную кислоту . Образующийся диоксид углерода сначала распадается на ионы H + и HCO3-. Они реагируют с амином. Абсорбированный CO 2 обратимо химически связан. Таким образом, химическое равновесие достигается только при значительно большей загрузке моющего средства. Этот механизм также можно использовать для объяснения селективности амина в отношении газового компонента.
Использует
В частном случае промышленного синтеза аммиак, для паровой риформинг процесс углеводородов для производства газообразных водород Обработка амином является одним из обычно используемых процессов для удаления избытка диоксида углерода при окончательной очистке газообразного водорода.
в биогаз при производстве иногда необходимо удалить из биогаза двуокись углерода, чтобы сделать его сопоставимым с природным. Удаление иногда высокого содержания сероводорода необходимо для предотвращения коррозии металлических деталей после сжигания биогаза.
Улавливание и хранение углерода
Амины используются для удаления CO2 в различных областях, от добычи природного газа до пищевой промышленности и производства напитков, и существует уже более шестидесяти лет.
Существует несколько классификаций аминов, каждая из которых имеет разные характеристики, относящиеся к CO.2 захватывать. Например, моноэтаноламин (MEA) сильно реагирует с кислыми газами, такими как CO.2 и имеет быстрое время реакции и способность удалять высокий процент CO2, даже при низком уровне CO2 концентрации. Как правило, моноэтаноламин (МЭА) может улавливать от 85% до 90% CO.2 из дымовых газов угольной электростанции, который является одним из наиболее эффективных растворителей для улавливания CO2.
Проблемы улавливания углерода с использованием амина включают:
- Газ под низким давлением увеличивает трудность переноса CO.2 из газа в амин
- Содержание кислорода в газе может вызывать разложение амина и образование кислоты.
- CO2 разложение первичных (и вторичных) аминов
- Высокое потребление энергии
- Очень большие помещения
- Поиск подходящего места для удаленного СО2
Парциальное давление является движущей силой переноса CO2 в жидкую фазу. При низком давлении такой передачи трудно достичь без увеличения тепловой нагрузки ребойлера, что приведет к увеличению затрат.
Первичные и вторичные амины, например MEA и DEA, будут реагировать с CO.2 и образуют продукты разложения. О2 от входящего газа также вызовет деградацию. Разложившийся амин больше не может улавливать CO.2, что снижает общую эффективность улавливания углерода.
В настоящее время синтезируются и тестируются различные смеси аминов для достижения более желательного набора общих свойств для использования в CO.2 системы захвата. Одно из основных направлений деятельности – снижение энергии, необходимой для регенерации растворителя, что существенно влияет на стоимость процесса. Однако необходимо учитывать компромиссы. Например, энергия, необходимая для регенерации, обычно связана с движущими силами для достижения высокой улавливающей способности. Таким образом, уменьшение энергии регенерации может снизить движущую силу и тем самым увеличить количество растворителя и размер абсорбера, необходимые для захвата заданного количества CO.2, таким образом, увеличивая капитальные затраты.