Что значит жесткость воды
Важнейшим свойством водопроводной воды является жёсткость. Данное качество сообщают ей соли кальция и магния, именуемые солями жёсткости. Чем меньше этих включений, тем вода будет мягче. Единая мера измерения жёсткости в мировом масштабе пока не установлена.
Согласно государственному стандарту ГОСТ 31865-2012 мерой жёсткости в Российской Федерации принят градус (º Ж), равный 1мг-экв/л (равно содержанию кальция или магния в концентрации ½ миллимоля на литр).
Чтобы соотнести градусные меры разных стран, в качестве условной принята единица пропромилле (ppm –part per million), т.е. миллионная часть (1·10−6) базовой массы: 1ppm=0,0001% (1мг/кг).
Что до бытовых приборов, то их показатели обычно указаны в единицах производителя. Для сравнения данных характеристик с нормативами, установленными в нашей стране, их переводят в российские единицы измерения.
Перевод градусов жёсткости в пропромилле:
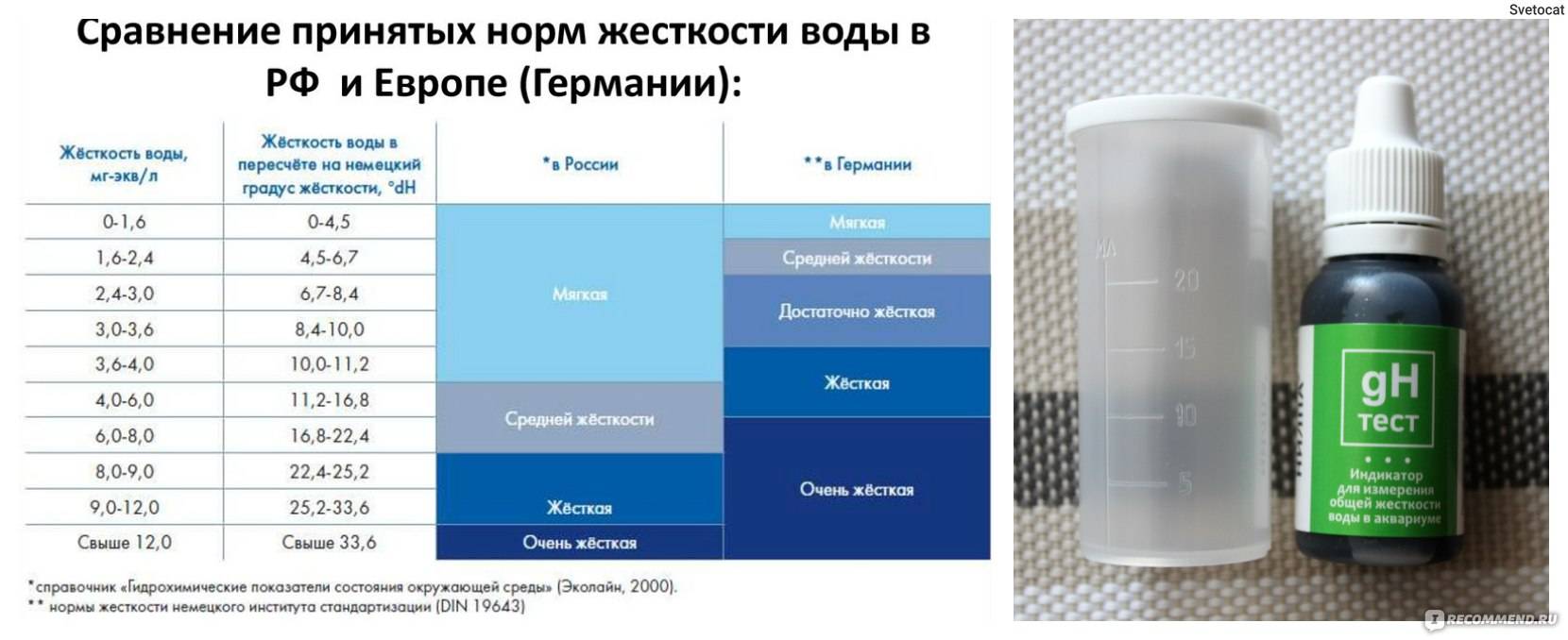
- 1 dH (Германия) = 17,8 ppm;
- 1 f (Франция) = 10 ppm;
- 1 (Англия) = 14,3 ppm;
- 1 A (США) = 1 ppm;
- 1 мг-экв/л (1ºЖ, Россия) = 50,05 ppm.
Известны три типа жёсткости:
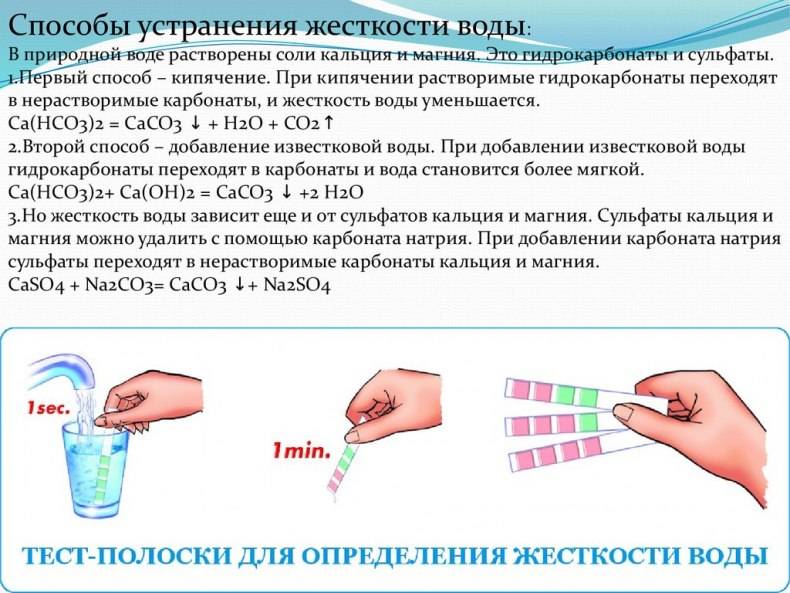
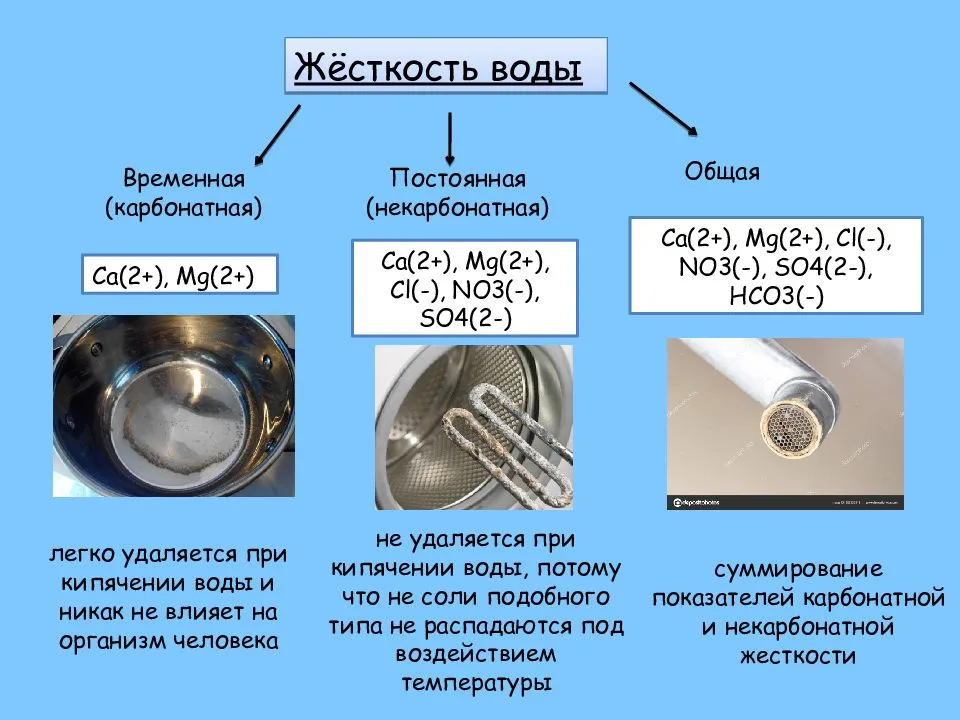
- Временная (или карбонатная), которая показывает содержание солей угольной кислоты (гидрокарбонатов Ca и Mg). При температуре кипения они распадаются, создавая нерастворяемый осадок СаСО3 (карбоната кальция) и Мg(OH)2 (гидроокиси магния).
- Постоянная (или некарбонатная), которая не растворяется при кипячении. Вода в этом случае содержит соли металлов с валентностью 2 (Ca, Mg, Ba, Sr), на основе сильных кислот: HCl (соляной), H2SO4 (серной), HNO3 (азотной). При установлении уровня жёсткости воды соли стронция (S) и бария (Ва) в расчет не принимают, так как их количество минимально;
- Общая, которая считается как сумма концентрации в воде ионов магния и кальция.
В нашей стране воду группируют по степени общей жёсткости:
- мягкая – до 2°Ж;
- средняя – 2-10 10°Ж;
- жёсткая – от 10°Ж.
Вас также может заинтересовать: Анализ питьевой воды: от сдачи проб до расшифровки результатов
Зачем определять жесткость воды

Вода содержит в себе растворенные соли щелочноземельных металлов, которые меняют ее физические и химические характеристики. Совокупность свойств воды, обусловленных наличием этих солей, и есть жесткость, которая является очень важным качеством жидкости. Жесткость воды определяют соли кальция и магния, так называемые соли жесткости. Чем меньше подобных примесей содержит вода, тем она мягче. На сегодняшний день в мире пока еще не существует общепринятой единицы измерения жесткости воды.
В России по государственному стандарту жесткость измеряется в градусах (Ж), при этом 1 Ж равняется 1 мг-экв/л (имеется в виду содержание солей кальция или магния, равное ½ миллимоля на литр). Для соотнесения градусных мер разных стран принята условная единица – пропромилле (ppm – part per million), то есть миллионная часть (1 10-6) базовой массы: 1 ppm = 0,0001 % (1 мг/кг).
В бытовых приборах, как правило, указываются единицы производителя. Чтобы определить, насколько эти показатели соответствуют установленным ГОСТом нормам, нужно перевести их в российские единицы измерения.

Перевод градусов жесткости в пропромилле:
- 1 dH (Германия) = 17,8 ppm;
- 1 f (Франция) = 10 ppm;
- 1° (Англия) = 14,3 ppm;
- 1 A (США) = 1 ppm;
- 1 мг-экв/л (1°Ж, Россия) = 50,05 ppm.
Существует три вида жесткости воды:
- Временная (карбонатная) – показывает содержание солей угольной кислоты (гидрокарбонатов Ca и Mg). Они распадаются при кипячении и создают нерастворимый осадок CaCO3 (карбоната кальция) и Mg(OH)2 (гидроокиси магния).
- Постоянная (некарбонатная) – когда вода содержит соли металлов с валентностью 2 (Ca, Mg, Ba, Sr) на основе сильных кислот: HCl (соляной), H2SO4 (серной), HNO3 (азотной). Они не выпадают в осадок под воздействием температуры кипения. При этом соли стронция (Sr) и бария (Ва) не учитываются в определении уровня жесткости воды, поскольку содержание их минимально.
- Общая – является суммой концентрации в воде ионов магния и кальция.
В Российской Федерации основой для подразделения воды на группы является общая жесткость:
- мягкая – до 2 °Ж;
- средняя – 2–10 °Ж;
- жёсткая – от 10 °Ж.
Опасность для человека, а также для нормального функционирования бытовой техники представляет как слишком жесткая, так и излишне мягкая вода. Вред мягкой воды не очевиден, но она может нанести непоправимый ущерб здоровью костей и зубов, вымывая из организма соли кальция. Кроме того, в ней быстрее распространяется коррозия металла в бытовых электроприборах. Чтобы предотвратить их разрушение, рекомендуется использовать ингибитор.
Негативные последствия использования жесткой воды:
- Способствует отложению солей в мочеполовой системе человека, вследствие этого образовываются камни в почках, состояние кожи и волос ухудшается. Если вовремя не определить уровень жесткости воды, появится налет внутри системы отопления и в канализационных трубах, что может привести к засорам и другим неприятностям, накипь скапливается внутри бытовых приборов, что неизбежно приведет к их поломке.
- Осадки солей жесткости препятствуют нагреванию ТЭНов, снижая их теплопроводность, поэтому электроэнергии для нагрева воды потребуется значительно больше. И, как следствие, нагревательные элементы сгорают, накапливая, но не выводя тепло должным образом.
- Расход моющих средств увеличивается, поскольку поверхностно-активные вещества (ПАВ) в них, взаимодействуя с солями кальция и магния, формируют нерастворимые соединения, мешающие образованию достаточного количества пены для удаления загрязнений.
- Канализационные трубы приходят в негодность из-за того, что их изнутри покрывает известковый налет, к тому же это может уменьшить напор в кране.
Важно своевременно определить жесткость воды из водопровода и других источников. Уберечь бытовую технику и водонагревательные приборы от поломок помогут различные смягчители воды

Важно определить, какие соли и в каком количестве присутствуют в используемой вами воде, прежде чем приобретать устройства и реагенты для ее смягчения
Обратите внимание, что различные явления природы, таяние снега и количество выпавших осадков могут повлиять на плотность солей, меняя тем самым общую жесткость воды. Рекомендуется сделать анализ на жесткость, чтобы подобрать смягчитель, подходящий конкретно для вашей воды
Для бытовых нужд, как то: стирка, уборка, мытье посуды и купание, вполне достаточно одного такого анализа, чтобы определить спектр необходимых средств. При избыточном содержании солей для готовки рекомендуется использовать очищенную воду в бутылях. Можно определить жесткость воды с помощью портативного прибора для обнаружения солей и карбонатов.

Читайте материал по теме: Чем опасен хлор в воде, и как решить эту проблему
Способы изменения жёсткости воды
Чтобы знать, в какую сторону производить изменения (повышать или уменьшать), определите жёсткость водопроводной воды и потребности ваших рыбок, может быть коррекции не потребуется вовсе.
Снижение общей жёсткости dGH
Способ № 1. Кипячение воды — поскольку в этом случае удаляется только карбонатная жёсткость, то общие значения изменяться не сильно. В зависимости от состава воды в вашем регионе колебания могут составить от пары процентов до 50% и более. Ориентируйтесь на потребности рыбок, возможно снижение жёсткости путём простого кипячения будет достаточно.Способ № 2. Вымораживание — данный способ актуален в условиях России с её длительной зимой. Воду заливают в ёмкость и выставляют на холод (например, на лоджию). Вода замерзает, начиная от стенок. В образующемся льде практически нет растворённых солей, они концентрируются в оставшейся жидкой воде, поэтому, когда лёд займёт 2/3 всего объёма, оставшуюся воду сливают, а лёд растапливают. В результате жёсткость снижается до 1-30dGH.Способ № 3. Пропустить воду через фильтр с обратным осмосом — вода после такой обработки очищается от всех примесей и становится практически дистиллированной. Перед применением в аквариуме полученную таким способом воду следует разбавить обычной водой.Способ № 4. Пропустить воду через ионообменные колонки — специальные смолы реагируют с солями кальция и магния, тем самым делая воду мягкой.
Повышение общей жёсткости GH
Жёсткость воды повышается довольно просто, например путём добавления кусочков известняка в аквариум или использования фильтров с мраморной крошкой в качестве фильтрующего материала, или применение химических реагентов: — хлорид кальция (CaCl2), продаётся в аптеках без рецепта, является лекарственным средством, а также зарегистрирован как пищевая добавка Е509; — сульфат магния (MgSO4), продаётся в аптеках без рецепта, является лекарственным средством.
Вода в аквариуме помутнела, что делать?
Вика Шарова
С водой после запущения мутнеет. Не бойтесь! Это установление биологического режима, проходит через 2-3 дня. Сначало используйте обязательно живые: кладофора шаровидная. Неделю подождите потом и рыб сажайте. А где-то через 2-3 дня можете выкинуть растение и купить пластиковые растения. А таких рыб можно поместить стаю 5-6 штук. Можно на несколько литров перенаселить аквариум обычно это определяется по пространству. А если не поместяца заведите маленьких красивых рыб: неонов. Содержат стаей, на 1 штуку 2 литра. А на ваш аквариум может поместица от 5 штук. Различие полов: у самца прямая полоска а у самки изогнутая у голубого неона. а бывают голубые, чёрные, красные неоны.
Дивергент
Воду не меняй ни в коем случае. Вот когда просветлеет (дня через 3-4), тогда и рыбок можно будет запускать. Это инфузории-туфельки размножились. По второму вопросу: Рыбам нужен кислород. Ставь тогда насос, если живых растений нет.
Наталья
Купите специальную жидкость для осветления аквариума. Она продается в зоомагазинах. Воду не надо менять, попробуйте подождать дня два, если не посветлеет добавьте эту жидкость, только немного (рыбкам от нее ничего не будет, проконсультируйтесь с продавцом).
Наталья А.
Так и должно быть на старте, ваше место в зрительном зале-ждать, когда пройдет вспышка, можете затемнить, фильтр ни в коем разе не отключайте, через пару тройку дней водичка сама очистится. Для барбусов, они стайные, объем мал, хотя вишневых пяток можно, не более, растения все же желательны живые и в вашем случае продувка. Никакую жидкость лить не советую, объем маленький и биологическое равновесие крайне неустойчиво, учитесь добиваться естественным путем.
определения общей жесткости с помощью обычного хозяйственного мыла
 Вариант Tetra Test
Вариант Tetra Test
Этот способ описал в своей книге И. Шереметьев. Основан этот метод на том, что хозяйственное мыло, как и любое другое трудно размылить в жесткой воде. И только когда мыло свяжет избыток солей кальция и магния – появляется мыльная пена.
Для определения жесткости воды нужно взвесить один грамм хозяйственного мыла, измельчить его и аккуратно, чтобы не образовалась пена растворить в небольшом количестве горячей дистиллированной воды. Дистиллированную воду можно купить в автомагазинах. Она используется для добавления в аккумулятор при повышении концентрации электролита.
Далее мыльный раствор наливаем в цилиндрический стакан и доливаем дистиллированной воды до уровня 6 сантиметров, если мыло 60% или до уровня 7 сантиметров если мыло 72%. Процент содержания мыла указан на бруске. Теперь в каждом сантиметре уровня мыльного раствора содержится количество мыла способное связать соли жесткости, количество которых соответствует 1°dH в 1 литре воды. Далее в литровую банку наливаем пол-литра исследуемой воды. И непрерывно помешивая, понемногу прибавляем наш мыльный раствор из стакана в банку с исследуемой водой. Поначалу на поверхности будут только серые хлопья. Затем появятся разноцветные мыльные пузыри. Появление устойчивой белой мыльной пены говорит о том, что все соли жесткости в исследуемой воде связаны. Теперь смотрим на наш стакан и определяем, сколько сантиметров раствора нам пришлось вылить из стакана в исследуемую воду. Каждый сантиметр связал в половине литра воды количество солей соответствующее 2°dH. Таким образом, если вам пришлось до появления пены вылить в воду 4 сантиметра мыльного раствора, то жесткость исследуемой воды равна 8°dH.
Если вы вылили в воду весь мыльный раствор, а пена так и не появилась, это означает, что жесткость исследуемой воды больше 12°dH. В таком случае исследуемую воду разбавляем дистиллированной водой в два раза. И проводим анализ снова. Теперь полученный результат жесткости нужно будет умножить на два. Полученное значение будет соответствовать жесткости исследуемой воды.
Стандартный стакан имеет объем 200 — 250 мл. Высоту около 10 сантиметров. Нижний диаметр от 55 миллиметров. Верхний диаметр 73 мм. То есть средний диаметр около 63 миллиметров. Если вы найдете химический цилиндрический стакан с подходящими характеристиками (диаметром около 6 сантиметров), то ваши измерения будут более линейными. Если цилиндра нет, то можно использовать и конусный. При этом неизбежно увеличение погрешности измерения. Но ведь и сам метод не эталон точности. С точностью до тысячных долей градуса жесткость определить этим методом не удастся, но оценить резкий уход общей жесткости от нормы с точностью 1 -2 °dH вполне возможно. При этом именно разность верхнего и нижнего диаметров сосуда, в котором находится мыльный раствор и дает эту погрешность в 1-2 градуса. Кроме переменного диаметра на погрешность влияет качество мыла, дистиллированной воды и ваш опыт использования данной методики. Если для pHпогрешность в 1 – 2 градуса может быть катастрофичной, то для общей жесткости такой разброс показаний вполне приемлем, он не приведет к гибели или нарушению здоровья обитателей вашего аквариума.
При определенном опыте погрешность метода около 1 – 2 °dH. Что вполне допустимо для наших целей. Учитывая простоту и доступность метода он, безусловно, заслуживает внимания.
Существуют и другие методы определения жесткости воды. Но одни из них сложны технически, другие требуют сложного оборудования, третьи не безопасны для домашнего использования. Поэтому я здесь о них не упоминаю. Как изменять жесткость воды рассмотрено в статье «Как устранить жесткость воды в домашних условиях«.
Жесткая и мягкая вода — в чем разница
Вода с большим содержанием таких солей называется жесткой, с малым содержанием — мягкой. Катионо-анионный состав, определяющий жесткость, приведен в таблице 1.
С помощью исследований было выявлено, что двухвалентные стронций, железо, марганец и барий несущественно изменяют значение жесткости, поэтому ими, как правило, пренебрегают. Алюминий Al3+ и трехвалентное железо Fe3+ также могут влиять на жесткость, но в обычных условиях они растворяются плохо, следовательно, их вклад в жесткость очень мал.
Параметры жесткости могут меняться в зависимости от того, какие полезные ископаемые распространены в данной местности, насколько хорошо они растворимы в воде и других факторов.
Негативное воздействие жесткой воды:
- вызывает образование накипи на промышленном и бытовом водонагревательном оборудовании (в том числе в чайниках, стиральных машинах и пр.), затрудняя их работу;
- плохо образует пену;
- сушит кожу;
- увеличивает время разваривания некоторых продуктов (круп, овощей) и др.
Использование слишком мягкой воды может приводить к коррозии труб из-за отсутствия нужного кислотно-щелочного баланса, поддерживаемого гидрокарбонатами.
Вкусовые качества жесткой воды также отличаются из-за наличия или отсутствия в ней различных солей:
- повышенное содержание солей магния, особенно сульфатов, может давать горечь;
- соли железа и марганца придают воде выраженный неприятный привкус, а при кипячении еще и бурый цвет;
- хлориды определяют соленость воды.
Многим людям кажется, что мягкая вода более приятна на вкус.
В некоторых источниках встречается информация, что употребление жесткой воды приводит к таким последствиям, как образование камней в мочеполовой системе, а мягкой — увеличивает риск сердечно-сосудистых заболеваний. Однако, достоверных клинических исследований или научных докладов, подтверждающих эти сведения, пока не проводилось.
Способы умягчения
Проверить уровень жёсткости можно несколькими способами, но это только половина дела. Конечно, если вода мягкая, то никаких дополнительных действий не потребуется, а вот повышенная жёсткость является проблемой, требующей устранения. Для этого применяются следующие методы:
- Термическая обработка (кипячение). Считается лучшим вариантом нейтрализации жёсткости, образованной гидрокарбонатами, но для остальных случаев не подходит.
- Очистка методом обратного осмоса. Способ основан на прохождении жидкости под давлением через полиамидные мембраны, проницаемые только для частиц, размер которых меньше диаметра молекул воды либо равен ему (например, кислорода). Вода проходит из более концентрированного раствора в менее концентрированный, то есть в обратном для осмоса направлении, вследствие чего очищается от большинства вредных примесей.
Очистка методом обратного осмоса поможет сделать воду менее жесткой Эффективность очистки может достигать 99,9%. Среди недостатков метода стоит отметить неизбежную предварительную подготовку подаваемой на мембрану жидкости.
- Реагентное умягчение, то есть добавление определённого количества соды либо гидратной извести. В этом случае щёлочноземельные соли переходят в нерастворимые соединения, впоследствии выпадая в осадок. Способ подразумевает точную дозировку реагента и последующую фильтрацию.
- Электродиализ — процесс изменения концентрации раствора путём выделения из него солей под воздействием электрического тока. Метод трудоёмкий и довольно затратный, поэтому применяется главным образом в промышленных установках.
- Катионирование — пропускание жидкости через специальный материал, называемый катионитом. В процессе фильтрации катионы, способствующие образованию накипи, поглощаются материалом и заменяются ионами натрия либо водорода. Одноступенчатое катионирование снижает уровень жёсткости до 0,05−0,1 °Ж, а двухступенчатое — до 0,01 °Ж.
В сутки человек употребляет не менее двух литров жидкости, качество которой оказывает непосредственное влияние на состояние его здоровья
Чистая вода с оптимальным содержанием необходимых микроэлементов помогает восстановить баланс в организме и обеспечить нормальную работу последнего, поэтому контролировать её характеристики чрезвычайно важно
Способы умягчения воды
- Самый простой и чудесный метод – элементарное кипячение воды, о котором было написано выше.
- Простейший химический способ – добавить гашенной извести.
Если два первых метода относились к карбонатной жесткости, то с постоянной жесткостью бороться сложнее. Но и это вполне реально:
- Вымораживание льда. Нужно не до конца заморозить воду и слить оставшиеся примерно 10%. Лед разморозить, он будет свободен от солей.
- Перегонка с испарением воды, так как соли не являются летучими веществами.
Теперь промышленные технологии избавления:
- Действие магнитных полей.
- Промышленная катионная очистка с реагентами и последующим определением карбонатной жесткости.
- Самый эффективный способ – осмос с фильтрами для обмена ионами, в результате чего «жесткие» соли заменяются на «мягкие».
Что такое жесткость воды
Говоря научным языком, жесткостью воды называют ее химические и физические свойства, которые зависят от количества растворенных солей жесткости, или щелочноземельных металлов – кальция и магния. Вода, где содержание этих элементов выше, считается жесткой, а там, где меньше – мягкой.
Особенности жесткой воды:
- после стирки белье приобретает жесткость, как после использования крахмала;
- на кожу такая жидкость оказывает высушивающий эффект, появляется ощущение стянутости, верхний слой начинает шелушиться;
- мыло в жесткой воде плохо вспенивается;
- на стенках кухонной посуды образуется осадок, особенно заметен он в чайниках и других нагревательных приборах.
Мягкая вода обладает рядом положительных качеств для кожи и волос человека, но имеет также и свои отрицательные стороны:
- мыльные растворы в мягкой воде отлично пенятся, но требуют большее количество жидкости для смывания;
- отсутствие накипи на элементах нагревания;
- в отличие от жесткой воды, не является причиной возникновения песка и камней, но способна провоцировать другие заболевания: кариес, гипертония, недостаток минералов, болезни ЖКТ;
- еда и напитки, приготовленные с использованием мягкой воды, имеют более приятный и выраженный вкус.
Как определить жесткость воды в домашних условиях

Если в чайнике постоянно появляется налёт, стиральная машина практически не удаляет загрязнения с одежды, посудомоечная машина не справляется даже с почти чистыми тарелками – стоит проверить уровень жесткости.
Также «симптомы» могут проявляться у владельцев квартиры, например, возникают проблемы с желудочно-кишечным трактом или чаще загрязняется кожа головы.
Определить уровень жесткости можно в лаборатории, при помощи специальных приборов и подручными средствами. Если у вас нет возможности предоставить пробу воды специалистам или приобрести ряд приспособлений, мы советуем использовать один из нижеприведенных способов.
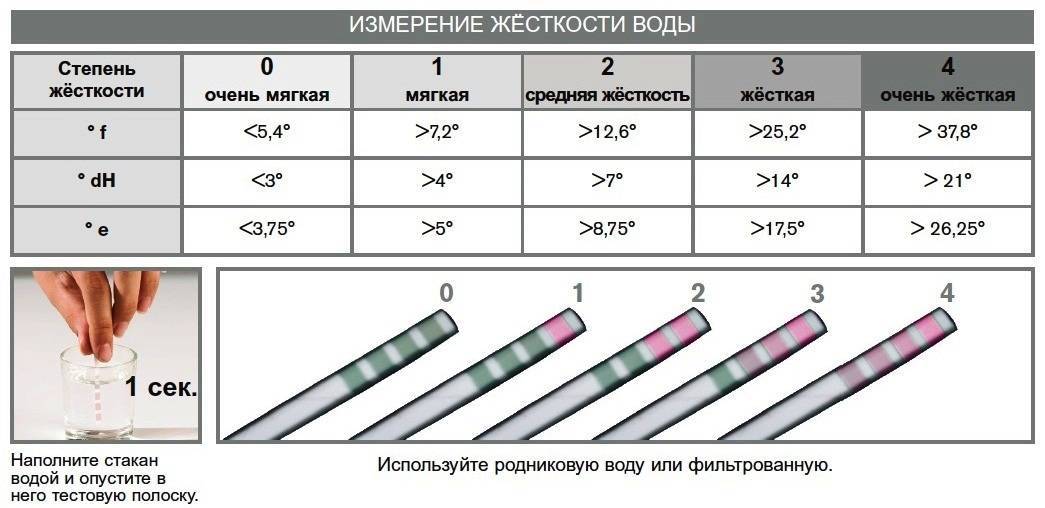
Измеряется уровень жесткости в °dH. Для проведения экспериментов вам пригодится следующая таблица:
| Очень мягкая вода | от 0 до 4 °dH |
| Мягкая вода | от 5 до 8 °dH |
| Средняя жесткость | от 9 до 18 °dH |
| Жесткая вода | от 19 до 30 °dH |
| Очень жесткая вода | от 31 °dH и выше |
Определение жесткости при помощи мыла
Понадобится кусок хозяйственного мыла. Из уроков химии мы знаем, что мыло плохо «работает» в жесткой воде, это обусловлено большим содержанием солей магния и калия в жидкости. Если вам не удаётся извлечь пену при намыливании рук – вода жесткая, когда появляется много пены и ее даже тяжело смыть – мягкая.
Для эксперимента также нужен прозрачный стакан. Лучше всего взять мерную емкость, где легко увидеть уровень жидкости. Если такой тары под рукой не оказалось, можно использовать и обычный стакан. Он может иметь диаметр от 55 до 75 миллиметров (5,5 и 7,5 сантиметров).
Проверка выглядит так.
- Необходимо взять 1 грамм мыла, измельчить и аккуратно растворить в дистиллированной воде, её можно приобрести в магазине. Далее мыльный раствор требуется перелить в цилиндрический стакан и долить воды – 6 см, если у вас мыло 60%, и около 7 сантиметров, если 72% (подобная информация указывается на упаковке мыла).
- В литровую банку нужно налить 0,5 л той воды, которую вы решили проверить. В эту же ёмкость вливаем полученную смесь из мыла дистиллированной воды, при этом постоянно помешивая.
- Сначала будут появляться только хлопья, но в дальнейшем образуются пузыри, потом на поверхности возникнет упругая белая пена. При её появлении смешивание прекращается, вам нужно перейти к измерениям. Для определения жесткости учитывается, сколько сантиметров воды пришлось вылить из стакана в банку для получения пены. Один сантиметр мыльного раствора приравнивается к 2°dH.
- Если вам потребовалось вылить 3 см до получения пены, ваша вода имеет жесткость 6°dH (мягкая). Если вы вылили весь мыльный раствор, а пены так и не появилось, вода определенно жесткая (выше 12 °dH).
- Для точной классификации можно повторить опыт, но разбавить образец смесью в два захода.
Обратите внимание, что подобный метод может давать небольшую погрешность в 1-2 градуса. При использовании обычного стакана вероятность неточности возрастает на несколько °dH
Подобный разброс вполне приемлем при домашней проверке воды.
По вкусу
Данный способ не гарантирует точного результата, но имеет право на существование. При должной сноровке вы сможете быстро отличить мягкую и жёсткую воду по вкусу с небольшой разницей (до 3-5°dH).
Для эксперимента потребуется три стакана. В первый наливается мягкая вода, обычно производители маркируют такие товары и их легко найти в магазине. Во второй следует налить вашу воду, в третью – с повышенным содержанием солей жесткости (например, лечебную или минеральную).
Для определения жесткости достаточно просто попробовать воду из каждого стакана и записать свои ощущения. Можно выстроить специальную шкалу, где на начальном этапе будет самая мягкая, а в конце – самая жесткая. На шкале отметьте точку, которая соответствует вашей воде (например, посередине или ближе к жесткой воде).
Зачастую используются баллы для домашней классификации: от 1 до 3 – мягкая; от 4 до 6 – средняя; от 7 до 10 – жесткая.